/reboot/media/9524b684-c4a9-11eb-9dc9-0242ac130004/82d45c8a-cfa8-11ed-a2f8-0242ac14000c/1-1-2aj9xm6.jpg)
Fibrillation Atriale en 2023 : mécanisme, symptômes, diagnostic et prise en charge
Communément mais improprement appelée « fibrillation auriculaire » ou « arythmie complète par fibrillation auriculaire », « AC par FA », la fibrillation atriale, dite FA, constitue un réel problème de santé publique.
Si vous êtes un médecin généraliste que vous souhaitez approfondir vos connaissances pour diagnostiquer une FA, découvrez un module ludique sur le portail réservé aux professionnels de santé.
Elle peut être résumée pour le médecin traitant par les dix les points clés suivants :
- C’est la maladie par trouble du rythme la plus fréquente. En France, sa prévalence est de 1 % de la population générale, 10 % au‑delà de 80 ans, 17% au‑delà de 85ans (*)
- A l’inverse des troubles du rythme ventriculaires de type Fibrillation ou Tachycardie Ventriculaires, la fibrillation atriale ne met pas en jeu le pronostic vital.
- Son risque n’est pas « rythmique » mais lié aux complications emboliques telles que l' Accident Vasculaire Cérébral (AVC) avec ses conséquences sur la qualité de vie et l’invalidité des patients.
- Le développement à long terme d’une complication de type insuffisance cardiaque par remodelage du cœur notamment le remodelage du ventricule gauche.
- Son dépistage par le médecin est le plus souvent facile.
- En présence de formes « fugaces », ou devant une complication, d'un AVC d’origine non précisée, le diagnostic de la fibrillation atriale est difficile à faire. Elle est mieux détectée par les nouvelles méthodes d’enregistrement longue durée de l’électrocardiogramme (ECG),
- La place du traitement antiarythmique est bien codifiée pour ralentir ou restaurer le rythme cardiaque
- Estimer la balance bénéfice‑risque du traitement anticoagulant par les scores
- La meilleure prise en charge du risque embolique par les nouveaux anticoagulants oraux directs (NOAC ou NACO) avec meilleur profil bénéfice‑risque/ AVK
- La transformation du traitement par les nouvelles techniques électrophysiologiques peu invasives dites «d’ablation ».
Comprendre la fibrillation atriale : Définition et mécanismes
Lorsque le cœur perd son rythme sinusal, la commande unique de l’impulsion au départ du nœud sinusal est laissée à de nombreux foyers anarchiques atriaux. L’oreillette peut atteindre jusqu’à 300 battements par minute.
Fort heureusement, la conduction est «freinée » par le nœud atrioventriculaire; la transmission au niveau du ventricule gauche se fait de façon rapide. Elle reste néanmoins moins rapide, anarchique et supportable par le patient. Au‑delà de 140 battements du ventricule gauche par minute, la tolérance est mauvaise.
Sur le tracé électrocardiographique, l’arythmie apparait sur toutes les dérivations. Elle se traduit par la perte du rythme sinusal remplacé par la traduction électrocardiographique de l’activité atriale anarchique. Le cœur bat irrégulièrement et rapidement. Les complexes issus du ventricule gauche (battements) sont irréguliers et plus ou moins rapides.
Quelles sont les causes d'une fibrillation atriale ?
La FA est due à des signaux électriques très rapides, désorganisés, ou chaotiques, provenant de plusieurs foyers ou à des circuits rotatifs, à partir d’impulsions siégeant dans les parois des deux oreillettes. L’abouchement des quatre veines pulmonaires dans l’oreillette gauche est le plus souvent à l’origine de ces foyers. Il constitue la cible prioritaire des ablations.
Au niveau de l’oreillette, la fibrillation entraîne un risque de stagnation du sang et la formation de caillots. Ces derniers peuvent migrer et entrainer des complications mettant en jeu le pronostic vital et fonctionnel du patient.
Le médecin pourra expliquer à ses patients en termes simples que « le sang n’est pas pompé efficacement dans le reste de l’organisme, ce qui peut provoquer une sensation de faiblesse ou de la fatigue ou des sensations cardiaques inconfortables comme des palpitations.
Le sang n’étant pas pompé efficacement dans l’oreillette. Il y séjourne plus longtemps et des caillots peuvent ainsi s’y former.
Ces caillots peuvent être ensuite dispersés dans la circulation .
Si un caillot atteint une artère du cerveau, il entraine un accident vasculaire cérébral.
C’est dire l’importance de l’anticoagulation, la fluidification de votre sang par des anticoagulants qui vont empêcher le caillot de se former, au détriment d’un risque hémorragique de saignement que l’on peut détecter : saignement du nez, dans les urines, en se brossant les dents, dans les fèces …et qu’ il faudra nous signaler immédiatement »
La fibrillation atriale en chiffre : Prévalence et impact
La fibrillation atriale est le trouble du rythme cardiaque le plus fréquent. En France, elle touche environ 1% de la population.
La fibrillation atriale (FA) touche fréquemment les personnes âgées et très âgées, avec une prévalence de 10 à 15 % après 80 ans. Ainsi, les données du Programme de médicalisation des systèmes d’information (PMSI) indiquent que 50 % des personnes hospitalisées pour FA sont âgés de 80 ans ou plus *.
C’est un réel enjeu de santé publique. Elle peut être dépistée par le médecin de ville, qui doit apprendre à mieux la connaitre.
Distinguer les types de fibrillation atriale : Classification et évolutions
Parfois précédée d’extrasystoles atriales (ESA), la fibrillation atriale par définition dure plus de 30 secondes.
Elle peut durer des heures, des jours voire des mois pour éventuellement devenir définitive.
Selon sa durée, et son allure évolutive, trois types d’ AC par fibrillation atriale ont été définies:
- La fibrillation atriale paroxystique dure < 1 semaine avec conversion (arrêt) spontanée ou par intervention en rythme sinusal normal. Les épisodes peuvent récidiver.
- La fibrillation atriale persistante est continue et dure > 1 semaine.
Une fibrillation auriculaire ancienne persistante qui dure > 1 an, mais avec encore la possibilité de restaurer le rythme sinusal.
- La fibrillation atriale permanente qui ne peut être convertie en rythme sinusal. Ce terme comprend également les personnes pour lesquelles une décision a été prise de ne pas tenter de conversion en rythme sinusal.
Nota Bene : Plus la fibrillation atriale est ancienne, moins une conversion spontanée en rythme sinusal est probable et plus la cardioversion est difficile du fait d'un phénomène de remodelage atrial. Apparaissent alors des modifications de l'électrophysiologie atriale, induites par le rythme rapide. Ces dernières sont dominées par une diminution de la période réfractaire de l’oreillette ; elles peuvent aussi comprendre une augmentation de la dispersion spatiale de la période réfractaire et/ou de la diminution de la vitesse de conduction atriale.
Origine et déclencheurs de la fibrillation atriale : Etiologie et facteurs favorisants
La FA peut être provoquée par une anomalie congénitale du cœur, dans les suites d’un infarctus myocardique ou en raison d’une maladie des valves cardiaques dite valvulopathie. Cette dernière recouvre les pathologies de la valve mitrale voire aortique.
La fibrillation atriale peut également apparaître chez les personnes sans antécédent particulier.
La probabilité de développer une arythmie complète par fibrillation atriale augmente rapidement avec l’âge.
Les causes les plus fréquentes de fibrillation atriale
Elles sont liées aux complications des affections suivantes
- L’hypertension artérielle +++
- Coronaropathie
- Cardiomyopathie
- Valvulopathies (sténose mitrale, insuffisance mitrale , insuffisance tricuspidienne )
- Hyperthyroïdie
- Intoxications alcooliques aigues
Les causes moins fréquentes :
-
Embolie pulmonaire
-
Communication interauriculaire et autres malformations congénitales
-
Bronchopneumopathies chroniques obstructives (BPCO)
-
Myocardite
- Péricardite
La fibrillation atriale solitaire, sans cause, est souvent retrouvée chez les sujets de moins de 60 ans
Diagnostic et dépistage clinique ou comment reconnaitre la fibrillation atriale
Le dépistage clinique peut être lié à des symptômes : le sujet se plaint de son cœur qui « saute dans la poitrine ».
Il peut être révélé par une complication liée à la migration d’un caillot de l’oreillette gauche vers une artère périphérique telle que celle du cerveau , œil , membre inférieur …
Symptômes
Au niveau du cœur, le malade ressent souvent ces palpitations anormales, battements irréguliers avec parfois une oppression thoracique , et /ou une fatigue à l’effort ( symptôme d’insuffisance cardiaque , la dyspnée d’effort apparait en particulier quand la cadence ventriculaire est rapide , 140 à 160 battements par minute , et est aussi liée à la perte de 10 à 20% de la contractilité cardiaque ).
A la prise du pouls (radial ou carotidien), les battements cardiaques sont irréguliers.
Il faut systématiquement prendre le pouls des patients en particulier âgés.
A l’inverse, certains patients ne ressentent aucun symptôme. Le dépistage de la FA relève d’une découverte fortuite lors d’un bilan cardiologique ou lors de la recherche d’une cause d’AVC.
L’accident vasculaire aigu peut révéler une fibrillation atriale.
Dépistage Paraclinique
Quels sont les examens qui font partie du bilan de la fibrillation atriale ?
Le dépistage paraclinique repose sur les analyses d’un ElectroCardioGramme, d’échographie cardiaque ou des tests des fonctions thyroïdiennes.
Comment reconnaitre une fibrillation atriale avec un tracé ECG ?
- A l’ECG , absence d’ondes P, présence d’ondes f ( de fibrillation ) insérées entre les complexes QRS , irrégulières polymorphes avec ondulations sur la ligne de base à plus de 300 par minute, visibles sur toutes les dérivations mais en particulier en V1
Les intervalles RR sont irréguliers et les QRS fins.
La traduction clinique en est l’irrégularité des battements du cœur.
- Les enregistrements ECG de longue durée permettent des diagnostics quand la FA est paroxystique ( Holter 24 h , 48 h voire huit jours ). Dans certains cas pour rechercher une cause d’ Accident Ischémique Transitoire (AIT) ou d’ AVC, l’implantation d’un REVEAL sous cutané est utile.
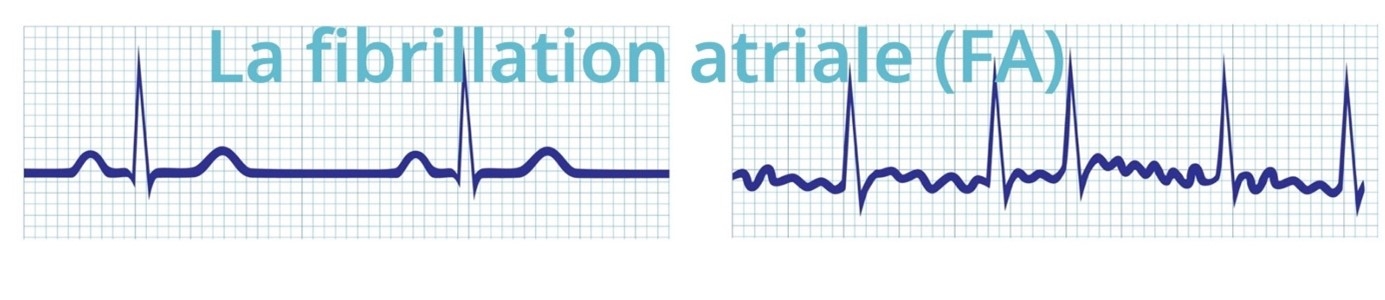
Nota Bene : Le flutter atrial est proche de la fibrillation atriale. Le flutter est un trouble du rythme atrial défini par son aspect souvent bien reconnaissable sur l'électrocardiogramme. Il s'agit d'une tachycardie régulière des oreillettes, se transmettant aux ventricules généralement avec une fréquence entre 200 et 300 par minute et des ondes en « dents de scie » caractéristiques
Comment reconnaitre une FA avec une échographie cardiaque ?
- Le cardiologue vérifie la taille de l’oreillette gauche, les éventuelles anomalies de la cinétique des parois ventriculaires gauches secondaires à un antécédent d'ischémie cardiaque une valvulopathie ou cardiomyopathie et identifiera les facteurs de risques d'AVC (stase ou thrombus intra‑auriculaire ou plaque athéromateuse aortique complexe).
Les thrombi ou caillots peuvent mieux être mis en évidence par une échocardiographie transœsophagienne .
Comment reconnaitre une FA avec les tests des fonctions thyroïdiennes ?
- dosage de TSH et recherche systématique d’une hyperthyroïdie.
Principes de la prise en charge et du traitement :
Il n’y a pas de traitement standard mais différentes stratégies thérapeutiques à adopter.
Doivent être pris en compte par le médecin,
- les trois différents aspects de la fibrillation atriale (paroxystique, persistante et permanente) leur tolérance ,
- leurs causes et pathologies sous‑jacentes
Le praticien doit apprendre à mieux évaluer la fibrillation atriale dans une approche multifactorielle.
Trois objectifs doivent être discutés
- Contrôler la fréquence cardiaque OU
- Contrôler le rythme cardiaque
- ET dans tous les cas, « anticoaguler », après avoir estimé le risque thromboembolique du patient
Le contrôle de la fréquence cardiaque peut être réalisé avec des médicaments antiarythmiques «ralentisseurs de la cadence du ventricule gauche » ou par ablation du nœud sinusal
Contrôle de la fréquence cardiaque: «ralentir le cœur»
Le contrôle de la fréquence cardiaque, moins de 100 battements/minute au repos, améliore les symptômes et prévient la cardiomyopathie induite par la tachycardie.
Pour les crises aiguës rapides avec une fréquence (ex. 140 à 160 battements/minute), les ralentisseurs du nœud auriculoventriculaire administrés par voie injectable sont utilisés, tels que l’amiodarone.
Les bêtabloquants tels que métoprolol, esmolol, sont préférés si on suspecte une composante adrénergique comme hyperthyroïdies ou pour les cas déclenchés par l'effort.
Les inhibiteurs calciques dihydropyridiniques tels que vérapamil, diltiazem sont également efficaces.
La digoxine est de moins en moins utilisée au vu de son efficacité. Mais elle reste un premier choix en cas d’insuffisance cardiaque concomitante.
Une fois l’urgence tachyarythmique passée, les mêmes médicaments peuvent être utilisés par voie orale pour contrôler la fréquence cardiaque au long cours. Il s’agit de bêta‑bloquants, inhibiteurs calciques non dihydropyridiniques de type verapamil ou diltiazem, digoxine, séparément ou en association.
En deuxième intention, l'amiodarone peut être proposée en surveillant sa tolérance notamment le risque d’hypo et d’hyperthyroïdie.
ATTENTION : en cas de syndrome de Wolf Parkinson White avec conduction auriculoventriculaire par une voie accessoire et QRS Larges, les médicaments bloquant la conduction au niveau du nœud auriculoventriculaire vont favoriser la transmission de l’influx par la voie accessoire avec risque de fibrillation ventriculaire fatale. Ils ne doivent pas être utilisés.
Contrôle du rythme cardiaque : «régulariser le cœur, avec retour au rythme sinusal » - La CARDIOVERSION
Le contrôle du rythme peut être réalisé par:
- des antiarythmiques,
- un choc électrique externe dite cardioversion synchronisée
ou
- l’ablation du substrat arythmogène de l’oreillette gauche.
En cas d’insuffisance cardiaque, la restauration du rythme sinusal est impératif. En effet, l’arythmie complète par FA diminue la fonction contractile et la Fraction d’éjection du ventricule gauche de 15 à 20%.
En l’absence d’insuffisance cardiaque le retour au rythme sinusal est souhaitable. Mais ce n’est pas une nécessité absolue .
De nombreuses études multicentriques ont évalué au long cours les antiarythmiques de classe Ia, Ic et III sur de grandes populations de patients en FA. Elles ont comparé les effets sur la morbimortalité de la restauration du rythme sinusal versus le ralentissement de la fréquence cardiaque sans retour au rythme sinusal.
Ils peuvent augmenter la mortalité (Etude CAST **)
En 2002 (Etude AFFIRM ***, NEJM 2002), il était établi que la restauration du rythme sinusal n’apportait qu’un bénéfice de confort pour le patient sans réduction de la morbimortalité. Or en 2020 l’étude EAST **** montre que restaurer le rythme sinusal réduit la morbimortalité des patients en FA.
La conversion en rythme sinusal ne dispense pas la prise d’anticoagulants.
Dans le cadre d'une conversion en phase aiguë, on peut utiliser soit une cardioversion par choc électrique externe (100 joules, suivie de 200 et 360 joules si nécessaire), soit médicamenteuse.
Avant que la conversion ne soit tentée, la fréquence ventriculaire doit être < 120 battements/minute et les patients bien anticoagulés .
La cardioversion est efficace dans 75 à 90% des cas.
Son efficacité et le maintien ultérieur du rythme sinusal une fois la procédure terminée est améliorée par l'administration au préalable (24 à 48 heures) d’antiarythmiques du groupe Ia, Ic ou III.
La cardioversion est efficace en cas de FA d'évolution courte, solitaire ou de cause réversible. Elle est moins efficace lorsque l'oreillette gauche est augmentée de volume (> 5 cm), ou en cas d’atteinte de la fonction cardiaque sous‑jacente.
La cardioversion peut être aussi réalisée après trois semaines si la fibrillation atriale est bien tolérée (sous anticoagulation préalable +++)
Anticoaguler, après avoir évalué le risque thrombo embolique :
Il doit être évalué en fonction du risque hémorragique, en fonction du terrain, des antécédents, de l’âge, à l’aide de scores CHADS Vasc et HASBLED établis à cet effet :
Le score CHA2DS2-VASc , permet d’évaluer la probabilité pour un patient ayant une FA sans pathologie valvulaire associée, d’être victime d’un AVC ischémique.
Il évalue ainsi la nécessité d’un traitement anticoagulant.
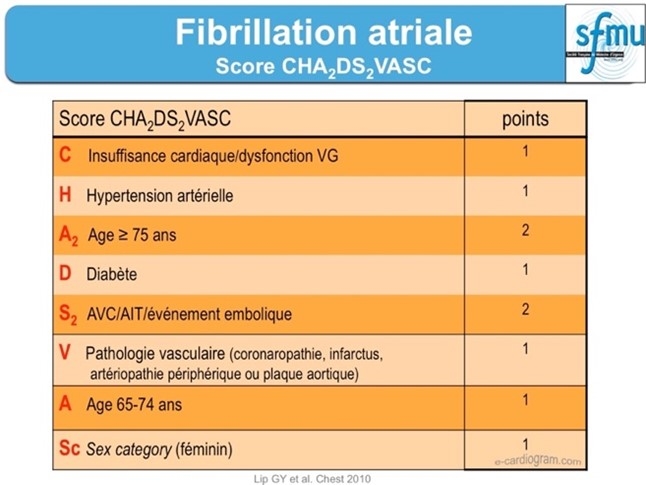
Réf: Société Française de Médecine d’Urgence .
Les anticoagulants réduisent le risque thromboembolique (TE) lié à une fibrillation atriale .
- Le risque estimé selon le score CHA2DS2‑VASc varie de 0 à 9 points, prédit une incidence annuelle d’AVC variable entre < 1 % et > 20 % (respectivement de « zéro à neuf points », de 0,8 ; 2,0 ; 3,7 ; 5,9 ; 9,3 ; 15,3 ; 19,7 ; 21,5 ; 22,4 ; 23,6 %) [2].
Soit environ x 2 jusque 4 , puis x3 de 5 à 9
- Il augmente pour une FA de durée plus 48 heures et après cardioversion (entre le 3e et le 30e jour).
L’estimation du risque thromboembolique (TE), quel que soit le rythme cardiaque au moment de l’examen (ex. conversion ou cardioversion) doit être systématique .
Elle repose sur le score CHA2DS2‑VASc (1): le risque TE, la première année de découverte d’une FA est x 2 , de 1 à 4 , puis x 3 au‑delà.
- Les facteurs de haut risque d’accident thromboembolique sont : un âge supérieur à 75 ans, un antécédent d’ AVC, d'AIT ou embolie systémique, un rétrécissement mitral ou la présence d’une prothèse valvulaire cardiaque mécanique.
Le Risque hémorragique est évalué par le score HAS‑BLED.
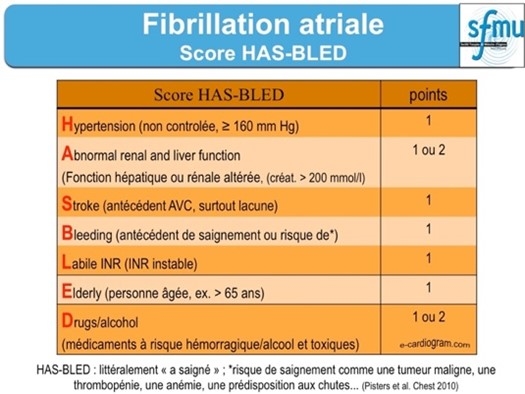
Réf :Société Française de Médecine d’Urgence .
- Si score HAS‑BLED ≥ 3, prudence et correction des facteurs de risque potentiellement réversibles de saignement. Le HAS‑BLED score ne doit pas être utilisé pour exclure les patients de la thérapie OAC. Mais il permet aux cliniciens de faire une évaluation éclairée du risque hémorragique.
- Le risque hémorragique doit être mis en balance avec le bénéfice attendu par un traitement AVK bien suivi : réduction d’environ 60% de l’incidence annuelle d’embolie systémique). Le bénéfice est d’autant plus fort que le risque primaire est élevé.
-
- Si le score HAS‑BLED est supérieur au score CHADS2, le risque hémorragique est supérieur au bénéfice potentiel d’une ACG orale . Un niveau élevé de score HAS‑BLED, soit à partir de 3 (taux d’accident élevé)
Les nouveaux anticoagulants oraux directs ont changé cette donne.
Quels patients anticoaguler et comment?
- Aucun traitement antithrombotique n'est recommandé en cas de FA non valvaire et de scores CHA2DS2‑VASc de 0 chez l'homme et de 1 chez la femme
- Ceux ayant une FA et une valve mécanique cardiaque sont traités par la warfarine. ( AVK ) +++
- Ceux ayant un rétrécissement mitral doivent être anticoagulés par la warfarine
- La vaste majorité de ceux avec une FA non valvulaire et qui doivent être traités par un anticoagulant oral, peuvent être traités soit par
- La warfarine avec un INR cible de 2,0 à 3,0, ( recommandation classe I )
- ou Les nouveaux anticoagulants oraux directs tels que apixaban, dabigatran, edxaban ou rivarxaban sont préférés aux antivitamines K, (type warfarine) car leur profil de tolérance prévention du risque thromboembolique / hémorragique est supérieur. De plus, ils ne nécessitent pas de contrôle permanent du degré de coagulation l’INR: recommandation de classe I
L’ablation
Une ablation du nœud auriculoventriculaire peut être pratiquée pour induire un bloc cardiaque complet chez le patient non répondeur ou qui ne supporte pas les médicaments.
Elle doit être suivie par l’implantation, l'insertion d'un stimulateur cardiaque permanent .
L’isolement électrique des veines pulmonaires de l'oreillette gauche peuvent prévenir une rechute en FA et éviter de provoquer un bloc auriculoventriculaire.
Son taux de réussite est d’environ 60 à 80% et son taux de complications de 1 à 5%. Cette procédure est souvent réservée aux meilleurs candidats comme les personnes jeunes sans cardiopathie sous‑jacente, FA résistante aux médicaments ou avec dysfonctionnement systolique ventriculaire gauche ou insuffisance cardiaque.
Conclusion
Une fois la FA diagnostiquée, le médecin détermine la meilleure attitude thérapeutique : restauration du rythme sinusal ou ralentissement de la cadence ventriculaire. La FA doit être traitée. L’anticoagulation reste au centre de la problématique pour prévenir le risque thrombo embolique notamment l'AVC.
Les nouveaux anticoagulants directs par leur optimisation du bénéfice‑risque apportent un nouvel éclaraige quant à la prise en charge médicamenteuse de la FA. Des molécules comme apixaban, dabigatran, edoxaban ou rivaroxaban montrent une réduction des AVC d’environ 30 % par rapport aux AVK.
Faut‑il restaurer le rythme sinusal pour un cœur en arythmie complète par fibrillation atriale en 2023?
En 2002 c’était mieux pour le confort et l’hémodynamique du patient. Mais cela n’améliorait pas la survie des patients en FA (Etude AFFIRM 2002 )
Depuis 2020, l'étude Européenne EAST, 1er septembre 2020 (P. Kirchhof et al)**** montre pour la première fois l’intérêt d’une prise en charge précoce et agressive de la fibrillation atriale avec pour objectif le contrôle du rythme cardiaque. Il en résulte une réduction significative de 21% des évènements cardiaques graves avec baisse de 28 % de la mortalité cardiovasculaire et de 35% de survenance d’un AVC.
Le contrôle du rythme cardiaque précoce et un retour du cœur en rythme sinusal est à l’origine de ce bénéfice quelle que soit la méthode utilisée pour l’obtenir - antiarythmiques avec ou sans ablation, elle‑même encadrée par l’utilisation d’antiarythmiques.
Bibliographie
*O.Hanon et al Revue du Praticien 2020
**CAST trial, Mortality and Morbidity in Patients Receiving Encainide , Flecainide, or Placebo -The Cardiac Arrythmia Suppression Trial , NEJM, 1991
*** AFFIRM trial , A comparison of Rhythm Control and Rate Control in patients with atrial fibrillation, The Atrial Fibrillation Follow‑up Investigation of Rhythm Management (AFFIRM) NEJM, 2002
**** EAST , P.Kirchoff et al NEJM 2020
:strip_exif()/reboot/media/9524b684-c4a9-11eb-9dc9-0242ac130004/2c5c0618-c51a-11eb-a911-0242ac130004-0f4d8df86cd0769f08050e129ad1ed29-edited/1-1-logo-intertio-2-06-2021-ai-2-1.png)
:strip_exif()/reboot/media/9524b684-c4a9-11eb-9dc9-0242ac130004/2c5c0618-c51a-11eb-a911-0242ac130004-0f4d8df86cd0769f08050e129ad1ed29-edited/1-1-logo-intertio-2-06-2021-ai-2-1.png)
/reboot/media/9524b684-c4a9-11eb-9dc9-0242ac130004/17b30164-eede-11ec-9d4d-0242ac14000a/1-1-img-20220617-174633.jpg)
/reboot/media/9524b684-c4a9-11eb-9dc9-0242ac130004/7ef7cc38-dc00-11ec-b344-0242ac140006/1-1-coqueluche.jpg)
/reboot/media/9524b684-c4a9-11eb-9dc9-0242ac130004/779c7ed4-34d4-11ed-8c68-0242ac14000b/1-1-d3955e.jpg)